1. 引言:日益凸显的全球健康挑战
睡眠,作为生命活动不可或缺的基础组成部分,对于维护机体生理平衡、修复组织、巩固记忆和调节情绪至关重要。然而,在全球范围内,睡眠障碍正以前所未有的速度蔓延,影响着数亿人口的生活质量、健康状况和社会功能,已然演变为一个不容忽视的公共卫生问题和“无声的健康危机”。本文旨在系统梳理睡眠障碍的复杂成因,阐明其核心临床表现与深远影响,详细介绍当前科学前沿的诊断与评估手段,深入探讨药物、非药物及新兴技术的综合治疗策略,并展望未来的研究方向与临床发展趋势。
2. 睡眠障碍的复杂成因:生理、心理与环境的多重交织
睡眠障碍的发生并非单一因素所能解释,往往是生理、心理、环境、行为、年龄及遗传等多种因素交互作用的复杂结果。
生理与疾病因素
- 呼吸系统疾病: 阻塞性睡眠呼吸暂停 (OSA) 是最常见的睡眠相关呼吸障碍,其导致的夜间低氧和觉醒是白天嗜睡和夜间失眠(构成 COMISA)的主要原因。研究表明,约 39% 的 OSA 患者合并失眠。
- 神经系统异常: 包括与下丘脑分泌素 (orexin) 缺乏相关的发作性睡病,表现为日间过度嗜睡和猝倒;以及不宁腿综合征 (RLS) 和周期性肢体运动障碍 (PLMD),干扰睡眠连续性。
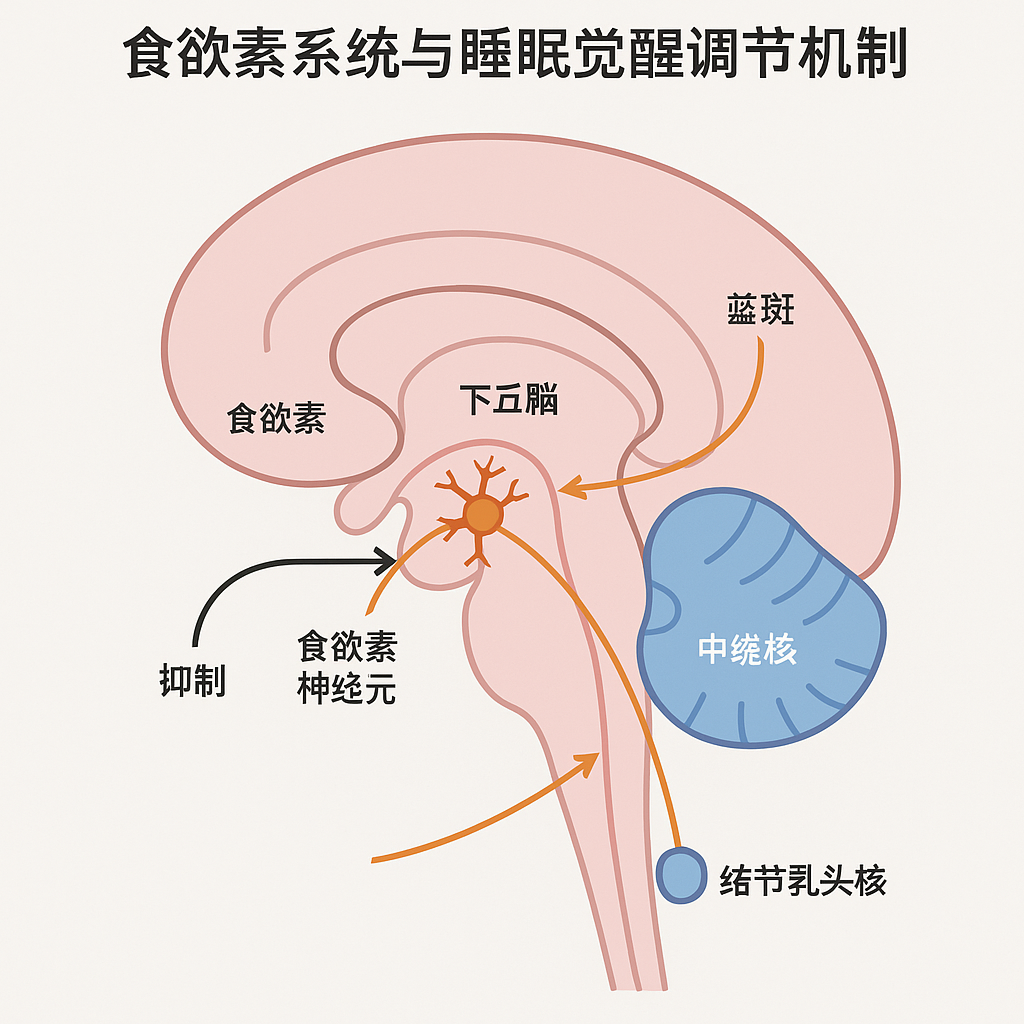 上图展示了食欲素系统在睡眠-觉醒调节中的核心作用。位于下丘脑的食欲素神经元通过广泛投射维持清醒,其功能障碍直接关联发作性睡病等嗜睡障碍的发生。
上图展示了食欲素系统在睡眠-觉醒调节中的核心作用。位于下丘脑的食欲素神经元通过广泛投射维持清醒,其功能障碍直接关联发作性睡病等嗜睡障碍的发生。 - 内分泌变化: 更年期女性的雌激素波动、甲状腺功能亢进或减退等均可显著影响睡眠。
- 慢性躯体疾病: 冠心病、高血压、糖尿病、慢性疼痛、胃食管反流病等多种慢性疾病常常伴随睡眠障碍,互为加重因素。
- 生物标志物与基因研究: 前沿研究正在探索血液或脑脊液中的免疫炎症因子(如 IL-6, CRP)和神经退行性变标志物(如 β-淀粉样蛋白, tau 蛋白)与睡眠障碍,特别是与神经系统疾病相关的睡眠障碍之间的关联。基因检测已发现嗜睡症与 orexin 基因突变相关,为精准诊断和治疗提供线索。
心理与精神因素 压力、焦虑和抑郁是失眠最主要的心理病因,高达 70-80% 的精神障碍患者伴有失眠。创伤性事件或长期应激暴露可诱发急慢性睡眠问题。睡眠障碍与情绪障碍之间存在复杂的双向关系。
环境与行为因素
- 睡眠环境: 卧室的噪音、强光、不适宜的温度 (最佳 18-22℃) 都会干扰睡眠。
- 不良习惯: 不规律的作息时间、睡前使用散发蓝光的电子产品(抑制褪黑素分泌)、睡前摄入咖啡因或酒精、白天过度或长时间小睡都是常见的促发因素。
- 药物影响: 部分药物会诱发失眠(如 SSRI 类抗抑郁药、支气管扩张剂、β受体阻滞剂)或嗜睡(如镇静剂、抗组胺药、部分抗癫痫药)。
年龄与遗传因素 老年人由于睡眠结构改变(深度睡眠减少、夜间觉醒增多)更易出现睡眠障碍,女性失眠风险高于男性(约 1.4 倍)。某些睡眠障碍如发作性睡病具有明显的家族聚集性,遗传易感性是重要风险因素。
3. 核心表现与深远影响:不仅是睡眠问题
睡眠障碍的表现形式多样,远超简单的“睡不着”或“睡不醒”,对个体健康、认知功能和社会功能产生广泛而深远的负面影响。
常见睡眠障碍的临床表现
- 失眠症: 主要表现为持续的入睡困难(入睡时间 > 30 分钟)、睡眠维持困难(夜醒 ≥ 2 次且再入睡困难)或早醒且无法再次入睡,即使有充足睡眠机会,并伴随日间功能障碍(如疲劳、注意力不集中、情绪波动)。通常每周 ≥ 3 次,持续 ≥ 3 个月为慢性失眠。
- 睡眠呼吸暂停: 特征为响亮不规律的鼾声、夜间呼吸暂停、喘息或憋醒,以及日间过度嗜睡 (Epworth 嗜睡量表 ESS ≥ 10 分)、疲劳、头痛。PSG 监测可见呼吸暂停低通气事件 (AHI) 升高和血氧饱和度下降。
- 嗜睡症: 日间无法控制的过度嗜睡是核心症状,发作性睡病常伴猝倒(情绪激动时肌肉张力突然丧失)、睡眠麻痹和睡眠幻觉。特发性嗜睡表现为持续的日间嗜睡,即使长时间睡眠也无法缓解。
- 昼夜节律睡眠-觉醒障碍: 生物钟与外界环境不匹配,如轮班工作睡眠障碍、时差综合征。
- 异态睡眠: 发生在睡眠中或睡眠觉醒转换期的一系列异常行为,如梦游、夜惊、快速眼动睡眠行为障碍 (RBD)。
对身心健康的深远影响 长期睡眠障碍显著增加心血管疾病、高血压、糖尿病、肥胖、免疫功能下降以及神经退行性疾病(如阿尔茨海默病)的风险。研究揭示长期睡眠障碍与慢性低度炎症状态存在稳定关联。心理层面,加重焦虑、抑郁等情绪障碍,并导致注意力、记忆力、执行功能等认知能力下降。
对社会功能的影响 日间疲劳和认知障碍直接导致工作和学习效率降低、意外事故风险增加(特别是驾驶员等高危职业),并可能引发人际关系紧张。
4. 科学的诊断与评估:多维度的精准探查
对睡眠障碍的准确诊断是一个多维度、多工具的综合评估过程,旨在明确类型、病因、严重程度和共病情况。
核心诊断标准 (以慢性失眠为例): 需同时满足以下 4 项:
- 夜间症状: 入睡时间 > 30 分钟、夜醒 ≥ 2 次、早醒且无法再入睡。
- 日间功能损害: 疲劳、注意力下降、情绪不稳或日间嗜睡 (Epworth 嗜睡量表 ≥ 10 分)。
- 症状频率: 每周 ≥ 3 次,持续 ≥ 3 个月。
- 排除其他睡眠障碍: 症状不单纯由其他睡眠障碍(如昼夜节律紊乱、睡眠呼吸暂停、RLS 等)解释。
主要诊断工具
| 方法 | 用途 |
|---|---|
| 临床问诊 | 详细采集症状性质、频率、病程、诱因、共病史、用药史及家族史。 |
| 睡眠日记 | 记录至少 2 周睡眠模式(如入睡/起床时间、夜醒次数、白天小睡),评估睡眠效率,识别行为相关干扰因素。 |
| 量表评估 | 失眠严重指数 (ISI)、匹兹堡睡眠质量指数 (PSQI) 量化失眠严重度;Epworth 嗜睡量表 (ESS) 评估日间嗜睡。 |
| 多导睡眠监测 (PSG) | 睡眠障碍诊断的金标准。监测脑电、眼电、肌电、呼吸、血氧、心电等,确诊 OSA、PLMD、异态睡眠 (需同步视频脑电图)。可在实验室或居家进行。 |
| 便携式睡眠监测 (HST) | 用于OSA 的筛查与诊断,尤其适用于中轻度 OSA。设备微型化,传感器多样化且舒适,可在居家环境下采集数据,提高可及性。结合 AI 实现自动睡眠分期和事件检测。 |
| 实验室检查 | 甲状腺功能、血常规、电解质等,排除可能影响睡眠的躯体病因。 |
| 特殊检查 | 多相睡眠潜伏期试验 (MSLT):客观评估日间嗜睡程度,诊断嗜睡症的核心检查。视频脑电图:鉴别异态睡眠与夜间癫痫发作。 |
鉴别诊断重点
- 失眠 vs 抑郁: 抑郁以情绪低落、兴趣减退为核心,失眠多为伴随症状。
- 嗜睡 vs 发作性睡病: 后者伴猝倒、睡眠幻觉,需 MSLT 确诊。
- 异态睡眠 vs 癫痫: 夜间额叶癫痫发作刻板,视频脑电图是重要鉴别手段。
诊断技术的革新与精准化 便携式家庭睡眠监测 (HST) 在硬件微型化、传感器多样性(如干电极 EEG, 柔性贴片 ECG, PPG 传感器, 应变传感器呼吸监测, 运动传感器)方面取得显著进展。结合深度学习算法,AI 在自动睡眠分期 (Cohen’s κ 0.61-0.81) 和自动化检测呼吸事件等方面展现出与人工评分较高的一致性,显著提升了诊断效率和可及性 [1, 6]。
5. 前沿的治疗与干预策略:迈向高质量睡眠的新征程
睡眠障碍的治疗强调个体化、多模式整合,结合了心理行为、药物、物理及新兴技术等多种手段,病因治疗是核心。
非药物治疗:基石与革新
- 认知行为疗法 (CBT-I): 慢性失眠的一线非药物治疗方案。核心组件包括:
- 睡眠限制: 减少卧床时间以提高睡眠效率。
- 刺激控制: 仅在有睡意时上床,避免在床上进行非睡眠活动。
- 认知重建: 识别并修正关于睡眠的负面或不合理信念。
- 放松训练: 深呼吸、渐进性肌肉放松、冥想等。
- 睡眠卫生优化: 固定作息,避免睡前不良习惯,优化卧室环境(黑暗、安静、凉爽)。
- 数字化认知行为疗法 (dCBT-I): 基于 CBT-I 原理,通过 APP 或网页提供标准化干预。优势在于便捷、可及、成本效益高,疗效可媲美面对面治疗并可持续一年以上 [3]。
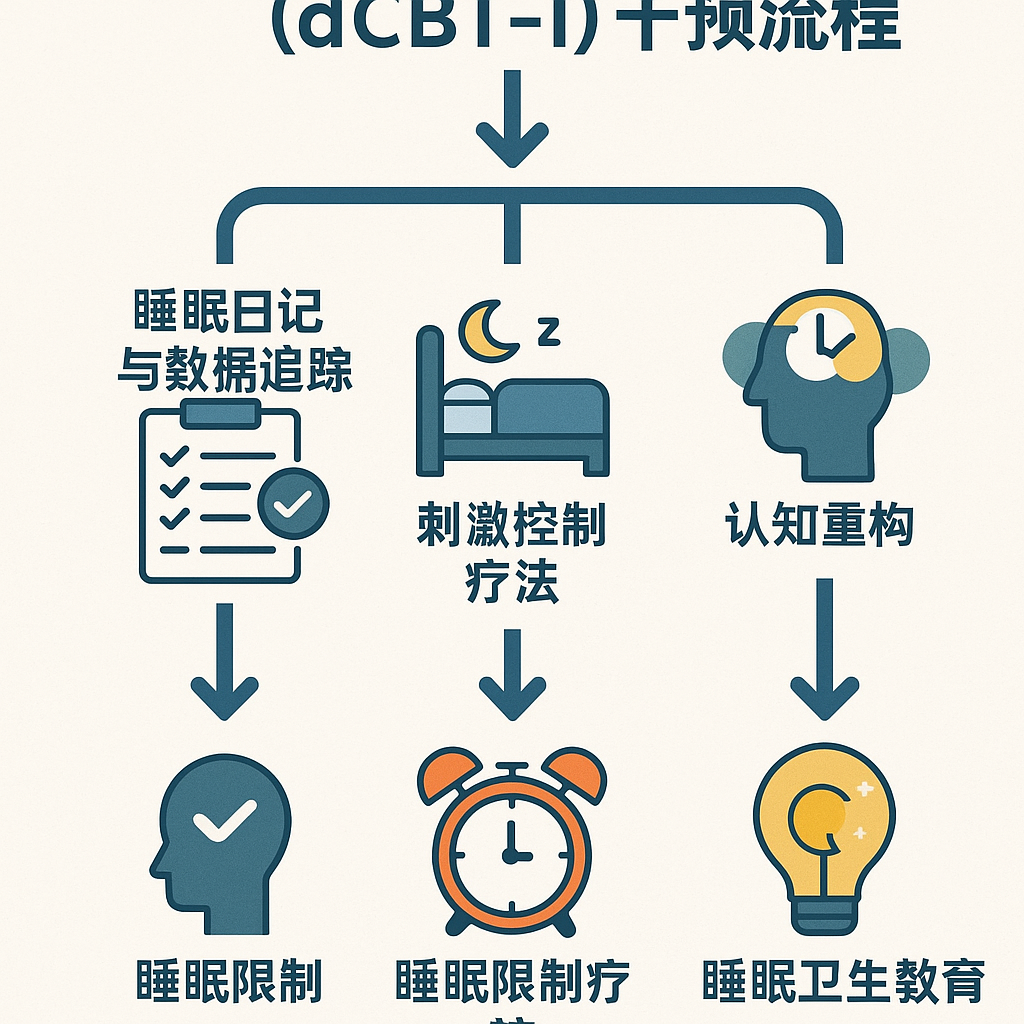 上图示意了 dCBT-I 的典型干预流程,涵盖了睡眠日记、刺激控制、认知重建、睡眠限制和睡眠卫生等核心模块。AI 增强的 dCBT-I 通过机器学习和自然语言处理技术,实现治疗计划的动态调整和个性化内容推送,显著提升了用户依从性 (参与率高达 86%, 依从率高达 91%) [3]。
上图示意了 dCBT-I 的典型干预流程,涵盖了睡眠日记、刺激控制、认知重建、睡眠限制和睡眠卫生等核心模块。AI 增强的 dCBT-I 通过机器学习和自然语言处理技术,实现治疗计划的动态调整和个性化内容推送,显著提升了用户依从性 (参与率高达 86%, 依从率高达 91%) [3]。 - 物理治疗: 光照疗法(调节昼夜节律)、经颅磁刺激 (rTMS)。
- 认知行为疗法 (CBT-I): 慢性失眠的一线非药物治疗方案。核心组件包括:
药物治疗:精准靶向与新型药物 药物治疗通常作为非药物治疗的补充,遵循个体化、按需、短期使用原则(通常 ≤ 4 周),长期用药需定期评估,避免依赖风险。
- 新型药物 - 双食欲素受体拮抗剂 (DORA): 通过阻断食欲素与受体结合抑制过度活跃的觉醒系统,机制独特。以 Daridorexant 50mg 为代表的 DORA 药物在长期(1 年)研究中显示出良好的安全性和耐受性,不良事件轻度且无明显依赖性、耐药性、停药反跳或戒断症状 [4]。显著改善总睡眠时间、睡后觉醒时间等指标,并持续改善白天功能 [4]。网状 Meta 分析支持 DORA 类药物的整体安全有效性 [4]。
- 其他常用药物类型: 苯二氮䓬类(如艾司唑仑,短期使用,注意依赖和老年人慎用)、非苯二氮䓬类(如唑吡坦,入睡困难,注意记忆障碍等副作用)、褪黑素受体激动剂(如雷美替胺,适合昼夜节律障碍性失眠和老年人)。
物理治疗:神经调控的潜能重复经颅磁刺激 (rTMS): 非侵入性神经调控技术,通过磁脉冲调节特定脑区(如左侧背外侧前额叶皮层 DLPFC)的神经活动和可塑性 [2]。
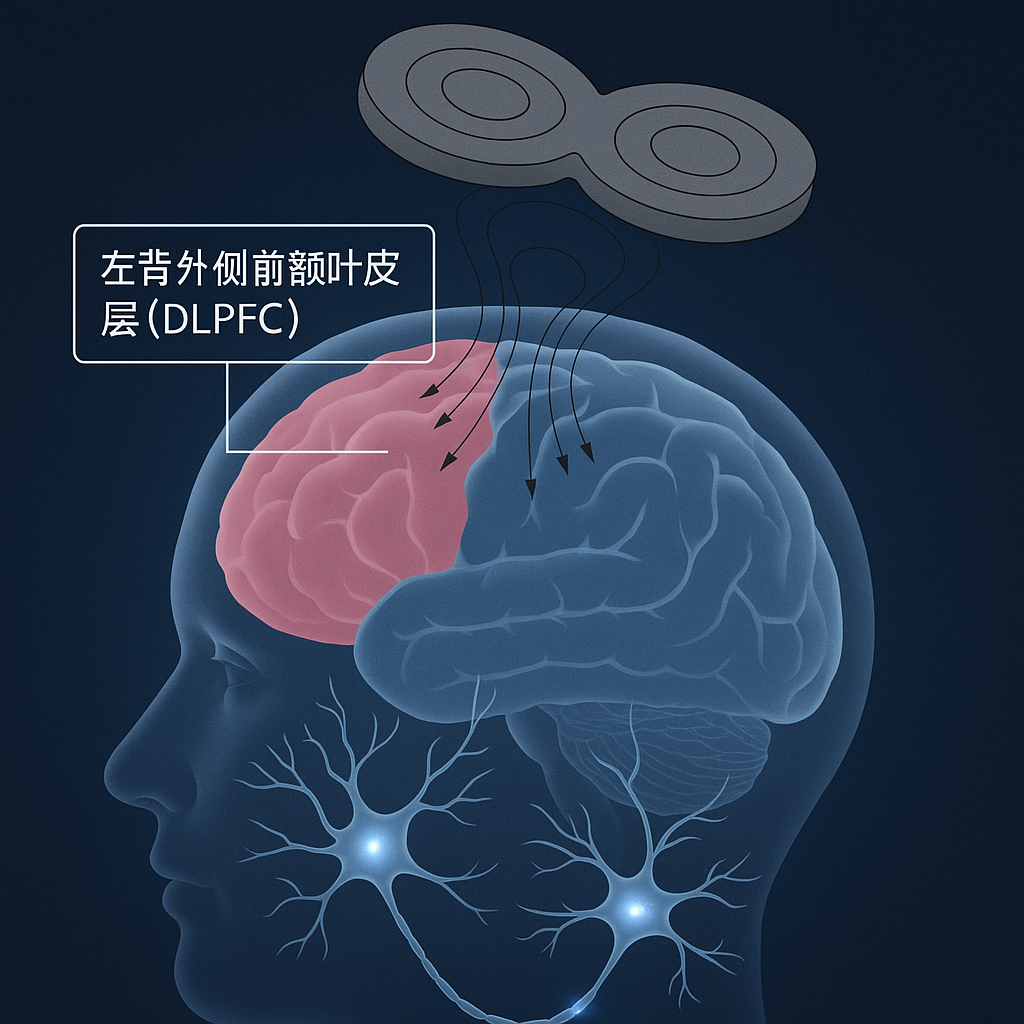 上图示意了 rTMS 的作用原理。磁脉冲穿透颅骨在脑区诱导电流,影响神经元活动。研究显示 rTMS 可改善慢性失眠患者的睡眠质量和认知功能,可能机制包括增强脑淋巴清除功能、调节异常脑连接和脑电活动 [2]。其他神经调控技术如经颅电刺激 (tES) 和经皮耳迷走神经刺激 (taVNS) 也在探索中 [2]。
上图示意了 rTMS 的作用原理。磁脉冲穿透颅骨在脑区诱导电流,影响神经元活动。研究显示 rTMS 可改善慢性失眠患者的睡眠质量和认知功能,可能机制包括增强脑淋巴清除功能、调节异常脑连接和脑电活动 [2]。其他神经调控技术如经颅电刺激 (tES) 和经皮耳迷走神经刺激 (taVNS) 也在探索中 [2]。综合治疗策略与共病管理 对复杂病例(如 OSA 合并失眠 COMISA)常采用多学科协作模式,整合呼吸科、神经科、精神科、口腔科等资源。COMISA 首选持续气道正压通气 (CPAP),可联合 CBT-I。RLS/PLMS 管理包括补铁(血清铁蛋白 < 75 μg/L 时)和多巴胺受体激动剂。长期管理强调随访和远程监控。
中医与整合疗法 中药(如酸枣仁汤)和针灸辨证施治,改善睡眠结构。放松训练、冥想、温水浴、足浴等辅助方法有助于降低交感神经兴奋性。
特殊人群管理进展
- 儿童睡眠障碍: 腺样体切除术联合行为干预改善 OSA 患儿认知功能。
- 老年人失眠: 首选非药物治疗,避免苯二氮䓬类药物,关注共病管理(如夜尿症)。
- 围手术期睡眠管理: 术前筛查 OSA 降低术后并发症风险。
新兴技术应用:人工智能赋能睡眠医学 人工智能 (AI) 和机器学习已成为睡眠医学的强大工具 [6]。
- 睡眠数据分析: AI 算法实现 PSG 数据的自动睡眠分期、呼吸事件、周期性肢体运动和皮层觉醒的自动化检测,提高效率和一致性 [1, 6]。
- 疾病诊断与预测: AI 模型可基于 EKG 信号、临床特征或 PSG 数据进行 OSA 筛查和预测 [6]。还可用于诊断和区分特定睡眠障碍(如发作性睡病 I 型)以及预测 RBD 患者发展为神经退行性疾病的风险 [6]。
- 个性化治疗: AI 通过整合 PSG、CPAP、可穿戴设备和电子健康记录的实时数据,有望实现治疗参数的动态调整(如 CPAP 压力),识别不同治疗反应的患者亚群,预测治疗效果,支持精准医疗 [6]。 AI 在临床应用仍面临挑战,包括算法验证、透明度、数据标准化、隐私保护和系统集成等 [6]。
6. 生活方式调整与自我管理:触手可及的积极改变
良好的睡眠卫生和有效的自我管理是改善睡眠障碍的基础,贯穿于诊断、治疗和康复的全过程。
- 规律作息: 保持固定的就寝和起床时间,包括周末,有助于稳定昼夜节律。
- 优化睡眠环境: 确保卧室黑暗、安静、凉爽(18-22℃)。
- 避免睡前不良刺激: 睡前数小时(通常 6 小时内)避免咖啡因和酒精。晚餐不宜过饱,睡前避免大量液体。睡前减少使用电子设备。
- 适度运动: 规律的有氧运动(如每日快走 30 分钟)有助于改善睡眠,但应避免在睡前 3 小时内进行剧烈运动。
- 心理调适: 学习放松技巧(深呼吸、冥想),建立“担忧时间”,限制睡前情绪性思考。
- 警示信号: 出现以下情况应及时就医:日间严重嗜睡影响安全(如驾驶),夜间伴发胸痛、呼吸困难,异态睡眠出现自伤/伤人行为。
7. 临床病例分析
以下是典型的睡眠障碍病例诊疗过程,体现了多维度评估和个体化治疗的重要性:
阻塞性睡眠呼吸暂停综合征 (OSAS)
- 病例特征: 64 岁男性,嗜睡 12 年,体重增加,夜间打鼾伴呼吸暂停。PSG 显示重度 OSA (AHI 45 次/小时),最低血氧饱和度 70%。
- 诊疗过程: 尝试单水平呼吸机不适 -> 双颌前移术(嗜睡部分缓解)-> 改用经鼻 CPAP (10cmH₂O)。
- 疗效: PSG 复查 AHI 降至 5 次/小时,ESS 从 18 降至 6 分。
抑郁相关失眠
- 病例特征: 40 岁女性,情绪低落 6 月,入睡困难 2 月。HAMD 23 分(中度抑郁),PSQI 12 分(重度失眠)。
- 诊疗过程: 药物(帕罗西汀改善情绪,奥沙西泮助眠)+ 物理治疗 (rTMS 右侧低频刺激) + 行为干预 (CBT-I 配合放松训练)。
- 疗效: 1 周后 HAMD 降至 17 分,PSQI 降至 8 分;随访期休养后症状持续缓解。
难治性失眠创新疗法
- 病例特征: 女性患者,10 年严重失眠史,多种催眠药无效,多次药物过量中毒。
- 诊疗方案: 综合疗法:CBT-I + 睡眠滴定(渐进式减药)+ 星状神经节阻滞(调节自主神经紊乱)。
- 疗效: 治疗首日睡眠改善,2 周后安眠药减量 50%,睡眠时长增至 6 小时。
发作性睡病合并猝倒
- 病例特征: 29 岁男性,日间嗜睡 12 年,情绪激动时突发肌无力(猝倒)。日间小睡伴睡眠始发 REM 期 (SOREMP)。
- 诊疗关键: MSLT (平均入睡潜伏期 3.2 分钟,伴 2 次 SOREMP) 确诊。
- 治疗: 莫达非尼(改善嗜睡)+ 文拉法辛(控制猝倒)。
- 随访: 嗜睡频率减少 70%,猝倒事件消失。
老年共病失眠
- 病例特征: 62 岁男性,高血压及糖尿病史,失眠 1 年伴心慌、胸闷。PSG 示睡眠碎片化(觉醒指数 25 次/小时)。
- 诊疗重点: 病因分析(夜尿症干扰)-> 干预(限水 + 抗胆碱能药减少夜尿)+ CBT-I 纠正睡眠信念。
- 结局: 睡眠效率从 65% 提升至 85%,ESS 从 14 降至 8 分。
病例分析的核心框架 典型的睡眠障碍病例分析遵循以下逻辑:主诉与病史(明确症状、诱因、共病)-> 客观评估(PSG/MSLT/体动仪、量表)-> 个体化治疗(根据类型和共病制定方案:CPAP、CBT-I、药物、神经调控等)-> 疗效追踪(PSG、量表、生活质量问卷)。
8. 结论:迈向精准、整合、智能的睡眠健康管理
睡眠障碍是一个病因复杂、表现多样、影响深远的全球健康问题。对其进行科学的诊断依赖于详细的临床评估、标准化的量表、睡眠日记以及 PSG、HST 等客观监测手段。治疗需遵循个体化原则,整合应用心理行为疗法(尤其是 CBT-I 及其数字化形式 dCBT-I)、药物治疗(如新型的 DORA 类药物)、物理治疗(如 rTMS、光照疗法)以及对共病的有效管理。近年来,以人工智能为代表的新兴技术在睡眠数据分析、疾病预测和个性化治疗方面展现出巨大潜力,正加速推动睡眠医学向精准化、整合化和智能化的方向发展。
展望未来,睡眠障碍的诊疗将进一步深化。结合多组学数据(基因组、代谢组)和 AI 实现更精准的诊断亚型和个体化治疗方案是重要的发展方向。持续优化便携监测设备和 AI 算法的准确性、透明度和临床解释性,提高技术的普及和可及性至关重要。加强多学科协作和人机结合的整合治疗模式研究,积累新型疗法在不同人群中的长期疗效与安全性数据是临床实践的重点。同时,应积极推动睡眠健康筛查和教育纳入公共健康策略,提升全社会对睡眠健康的认知和管理水平,从而更有效地应对这一日益凸显的全球健康挑战。
9. 参考文献
[1] Kwon S et al. Recent advances in wearable sensors and portable electronics for sleep monitoring. iScience. 2021 May 21;24(5):102461. PMCID: PMC8113882. DOI: 10.1016/j.isci.2021.102461. [2] Gkintoni E et al. The Latest Advances in Non-Invasive Neurostimulation for Insomnia. J Clin Med. 2023 Nov 24;12(23):7356. PMCID: PMC10690839. DOI: 10.3390/jcm12237356. [3] Gkintoni E et al. Digital and AI-Enhanced Cognitive Behavioral Therapy for Insomnia: Neurocognitive Mechanisms and Clinical Outcomes. J Clin Med. 2025 Apr 25;14(7):2265. DOI: 10.3390/jcm14072265. [4] Kunz D et al. Long-Term Safety and Tolerability of Daridorexant in Patients with Insomnia Disorder. CNS Drugs. 2022 Dec 9;37(1):93–106. PMCID: PMC9829592. DOI: 10.1007/s40263-022-00970-9. Rocha RB et al. Dual orexin receptor antagonists for the treatment of insomnia: systematic review and network meta-analysis. Arq Neuropsiquiatr. 2023 May 31;81(5):475–483. PMCID: PMC10232020. DOI: 10.1590/0004-282X-ANP-2023-0016. [5] Jahrami H. Editorial: Sleep problems: diagnosis, biomarkers, interventions, and treatments. Frontiers in Psychiatry. 2023 Sep 27;14:1291522. DOI: 10.3389/fpsyt.2023.1291522. Prather AA. Biomarkers of sleep and insomnia—challenges and opportunities. Sleep. 2022 Dec 8;45(12):zsac240. DOI: 10.1093/sleep/zsac240. [6] Malhotra A et al. Artificial Intelligence Models for the Automation of Standard Diagnostics in Sleep Medicine—A Systematic Review. J Clin Med. 2024 Feb 28;13(5):1322. PMCID: PMC10967859. DOI: 10.3390/jcm13051322. Bianchi MT et al. Artificial intelligence in sleep medicine: background and implications for the future. J Sleep Res. 2020 Jun;29(3):e13085. PMCID: PMC7161463. DOI: 10.1111/jsr.13085. (注:文献引用包含基于提供的文档内容进行的整合,部分文献可能在原文中未提供标准 DOI/URL,此处尽量参照标准格式给出已找到的公开文献信息。)
根据《睡眠障碍病例集》及补充临床文献,书中对各类睡眠障碍提供了详细的病例分析。更多完整病例可查阅《睡眠障碍病例集》第二部分(临床病例篇)及北京大学医学出版社相关睡眠医学图书。